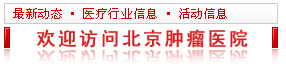
伦理委员会工作流程
复审流程

模板2(修改内容均标红,保留修订格式)
知情同意书
方案名称:
方案编号:
知情同意书版本号:12.0 ,20167年012月01日
研究机构:
主要研究者:
患者姓名: 患者姓名缩写:
患者地址:
患者电话:
我们在此邀请您参加一项临床试验。本知情同意书提供给您一些信息以帮助您决定是否参加此项临床试验。请您用一定的时间仔细阅读下面的内容,如有不清楚的问题或术语,可以与有关医师进行讨论。
您参加本项研究是完全自愿的。本次研究已通过北京肿瘤医院伦理委员会审查。
1. 研究背景:
…………
…………
…………
6. 参加研究的受益:
参加本研究你可能不受益,不能保证试验药物将会改善您的病情。因您参加本研究获得的信息可能在将来帮助其他患者。您也可能通过治疗方案得到疗效改善。研究期间我们将免费为您提供2周期的药物,研究过程将得到医生密切的关注。
7. 替代治疗
…………
…………
…………
12.样本保留
您的样本会在研究结束后保存数年,仅供用于研究目的。开展任何一项新的、与本研究无关的样本分析前,都要得到您的允许,这时会要求您签署一份新的同意书允许进一步使用样本。您有权拒绝。如果您退出研究,在您决定退出前已经采集的数据(和任何样本)可继续供研究使用。如果您选择将之前保留的样本销毁,必须书面通知研究医生。
…………
…………
…………